戴 青,张秀英,杨秀玉,韩宁宁,王 轩, 季 璇,赵 晖
(中国兽医药品监察所,北京 100081)
泰拉霉素是由美国辉瑞动物保健公司开发的动物专用新型大环内酯类抗生素,主要用于治疗牛和猪呼吸系统感染性疾病[1-2],目前临床上广泛应用的制剂为泰拉霉素注射液。泰拉霉素由15元氮杂内酯环(泰拉霉素A)和13元氮杂内酯环(泰拉霉素B)两种同分异构体组成[3],该两种同分异构体均是泰拉霉素中的抗菌活性成分,原料药中泰拉霉素B含量较少,但泰拉霉素A与泰拉霉素B这两个异构体在溶液中易发生转化,且处于平衡,需要以两个异构体之和对含量进行控制。目前,各国药典均未收载泰拉霉素原料药及相关制剂的质量标准,均无泰拉霉素国家标准物质供应,调研发现,在企业内部质量控制过程中,多使用自制工作对照品。因此,为了更好地对产品进行质量控制,研制了泰拉霉素国家对照品,对于泰拉霉素原料及注射液的生产及质量控制具有重要意义。
1.1 仪 器 e2695型高效液相色谱仪(美国Waters公司);
2489型紫外检测器(美国Waters公司);
2998型二极管阵列检测器(美国Waters公司);
AUTOPOL V型自动旋光仪(美国Rudolph公司);
TENSOR 27型傅里叶变换红外光谱仪(德国Bruker公司);
7890A型气相色谱仪(美国Agilent公司);
AX205型电子天平(美国Mettler公司);
701KF型水分测定仪(瑞士Metrohm公司);
DSC Q200型差示扫描量热仪(美国TA公司)。
1.2 试 药 原始发明厂泰拉霉素工作对照品(含量99.0%,美国Zoetis公司);
泰拉霉素原料由Zoetis公司生产;
甲醇、乙腈(色谱纯,德国Merk公司);
磷酸二氢钾(分析纯,中国上海源叶公司);
实验用水为超纯水。
2.1 样品制备 将精制后的泰拉霉素原料分装于棕色安瓿瓶中,每支100 mg,置于5 ℃冰箱储存,作为待标品,经理化分析、标定含量后贴签入库,作为国家对照品发放。
2.2 比旋度 取待标品适量,用乙腈溶解制成40 mg/mL的溶液,采用钠光谱D线(589 nm),测定待标品溶液旋光度,测定结果为-25°。
2.3 红外光谱鉴别 分别取待标品与泰拉霉素工作对照品适量,用溴化钾压片,测定二者红外光吸收图谱,结果为二者红外光吸收图谱一致(图1~图2)。
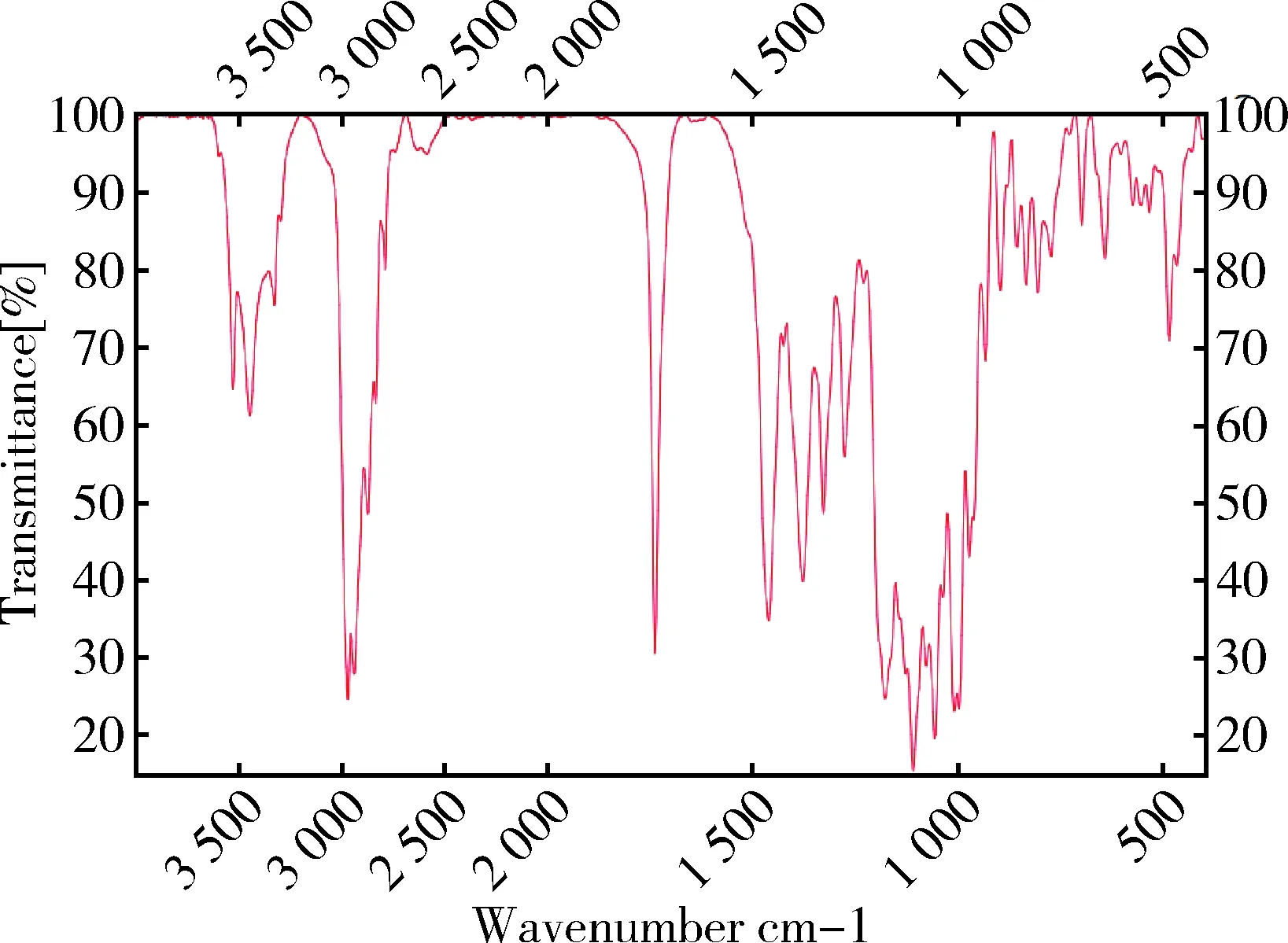
图1 泰拉霉素工作对照品红外光谱图Fig. 1 Infrared spectrum of tulathromycin working reference substance
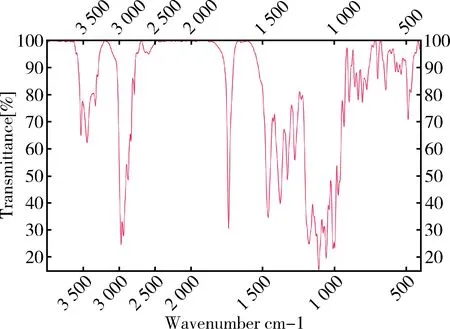
图2 本批泰拉霉素对照品红外光谱图Fig 2 Infrared spectrum of this batch of tulathromycin reference substance
2.4 有关物质
2.4.1 液相色谱条件 色谱柱Kromasil C18(4.6 mm×150 mm,3.5 μm);
以甲醇-乙腈-0.075 mol/L磷酸二氢钾溶液(pH 7.0)(45∶25∶30)为流动相;
流速1.0 mL/min;
检测波长205 nm;
柱温40 ℃。待标品溶液质量浓度为2 mg/mL,进样体积为25 μL。采用自身对照法计算有关物质,测得总有关物质量为1.38%。
2.4.2 方法专属性 按照上述方法,在待标品溶液中加入1 mol/L盐酸溶液,室温破坏2 h进行酸降解;
在待标品溶液中加入1 mol/L氢氧化钠溶液,室温破坏2 h进行碱降解;
在待标品溶液中加入3%双氧水溶液,室温破坏2 h进行氧化降解;
将待标品在120 ℃放置8 h进行高温降解;
将待标品在5000 lx光照下放置8 h进行光照降解。分别测定各种破坏性试验条件下待标品的有关物质,并采用二极管阵列检测器,进行峰纯度检查。破坏性试验结果见表1,结果表明,酸、碱、氧化降解均易增加杂质含量,提示样品应避免接触强酸、强碱、氧化剂等,以防止产生过量杂质。各条件下主峰均可与相邻峰实现良好分离,且各杂质峰纯度角度均小于阈值,为单一物质峰,降解产物不干扰主峰测定,表明方法专属性良好。
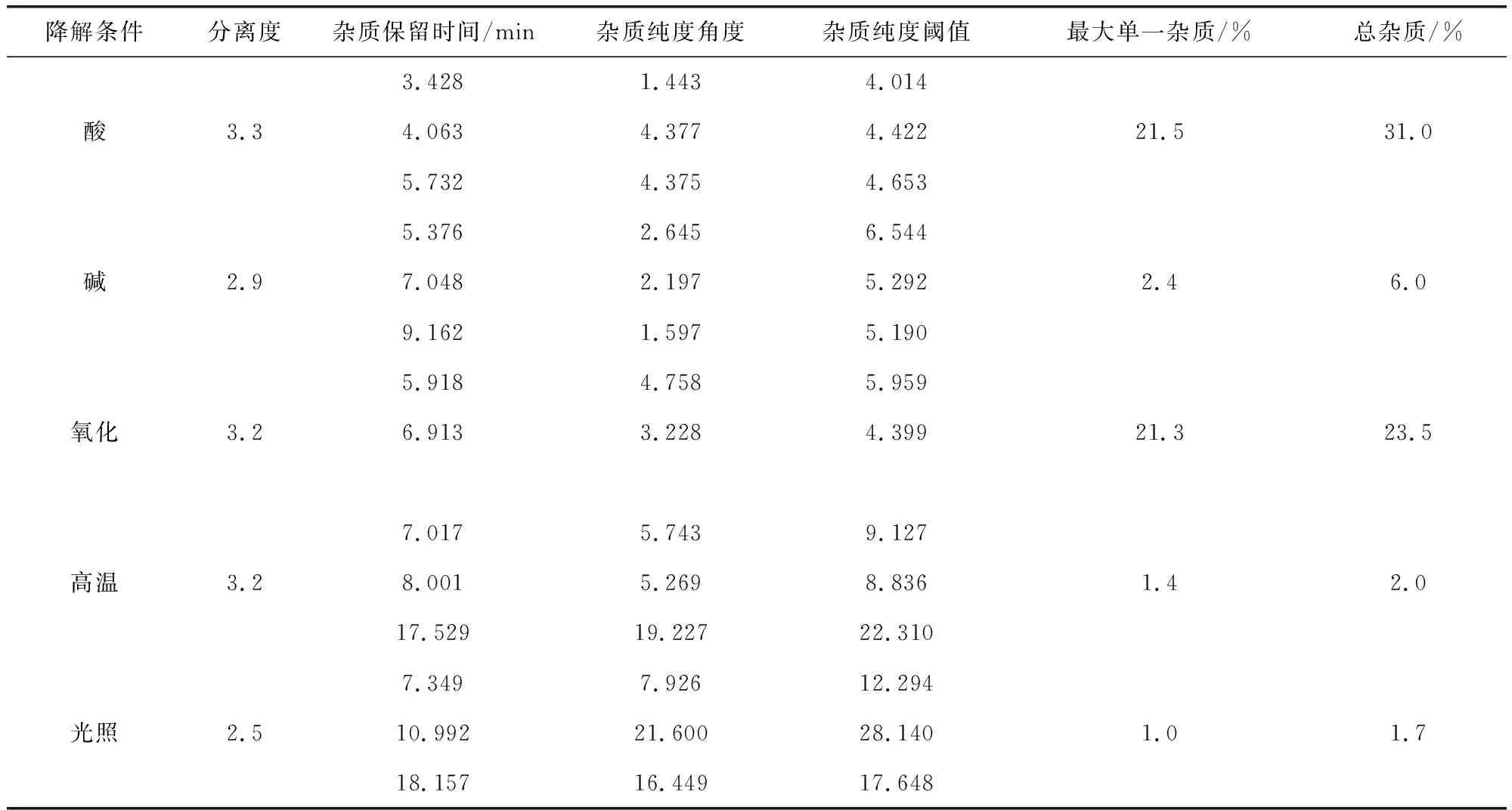
表1 破坏性试验结果Tab 1 Results of destructive tests
2.4.3 检测限 将2 mg/mL的溶液进一步稀释为1 μg/mL的检测限溶液,测定信噪比。检测限溶液信噪比为3∶1,表明该方法泰拉霉素的检测限为1 μg/mL。
2.4.4 线性与范围 配制10 mg/mL的贮备液,经一系列精密稀释,分别制成5000、2000、1000、400、100、10、2 μg/mL的溶液,采集色谱图,以峰面积与浓度作图,用最小二乘法进行线性回归。峰面积与浓度线性方程为:y=3414.7x-5881.9,r=1。表明在2~5000 μg/mL范围内浓度与峰面积具有良好的线性关系。
2.4.5 溶液稳定性 将溶液于室温放置12 h,期间不同时间进样采集色谱图,考察峰面积变化情况。溶液稳定性结果见表2,峰面积12 h内RSD为1.6%,小于2.0%,表明该溶液室温放置12 h稳定性良好。
2.5 液相色谱鉴别 分别取待标品与泰拉霉素工作对照品适量,按照2.4.1项下色谱条件,测定二者主峰的保留时间,结果为样品高效液相色谱图主峰保留时间与泰拉霉素工作对照品的保留时间一致,且溶剂空白对泰拉霉素测定无干扰(图3~图5)。
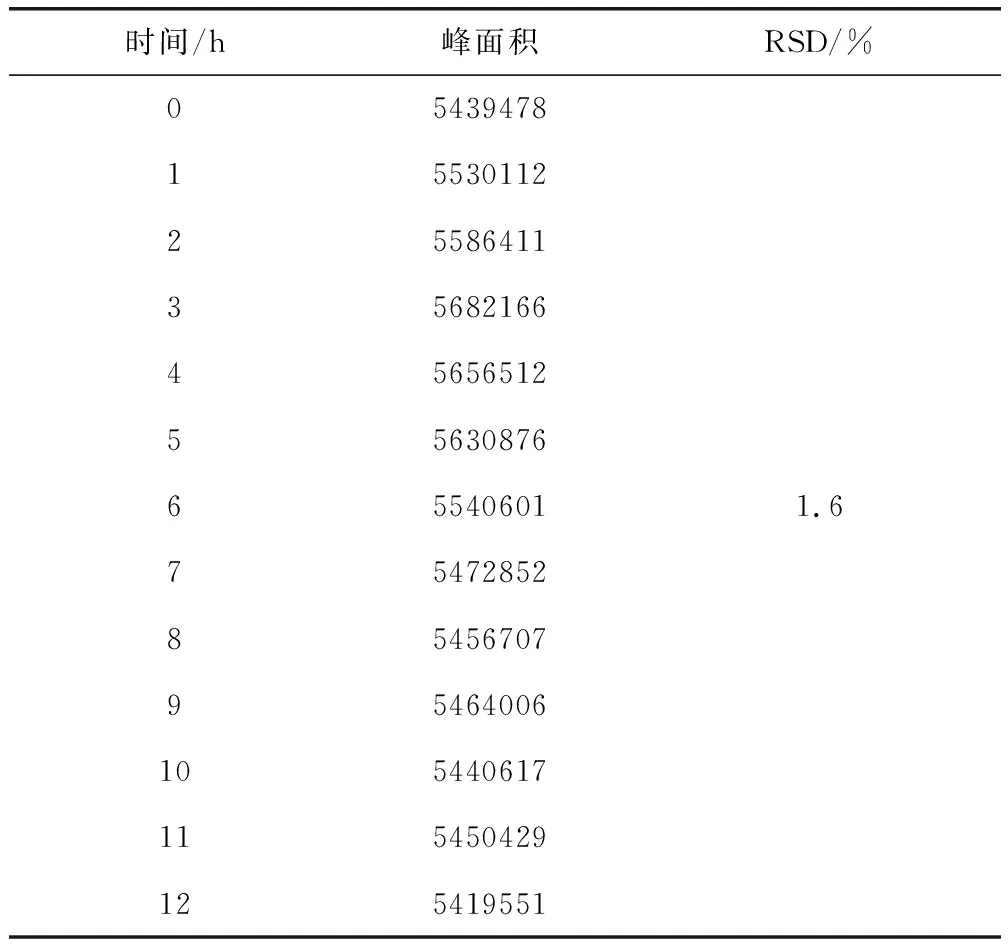
表2 溶液稳定性结果Tab 2 Results of solution stability test
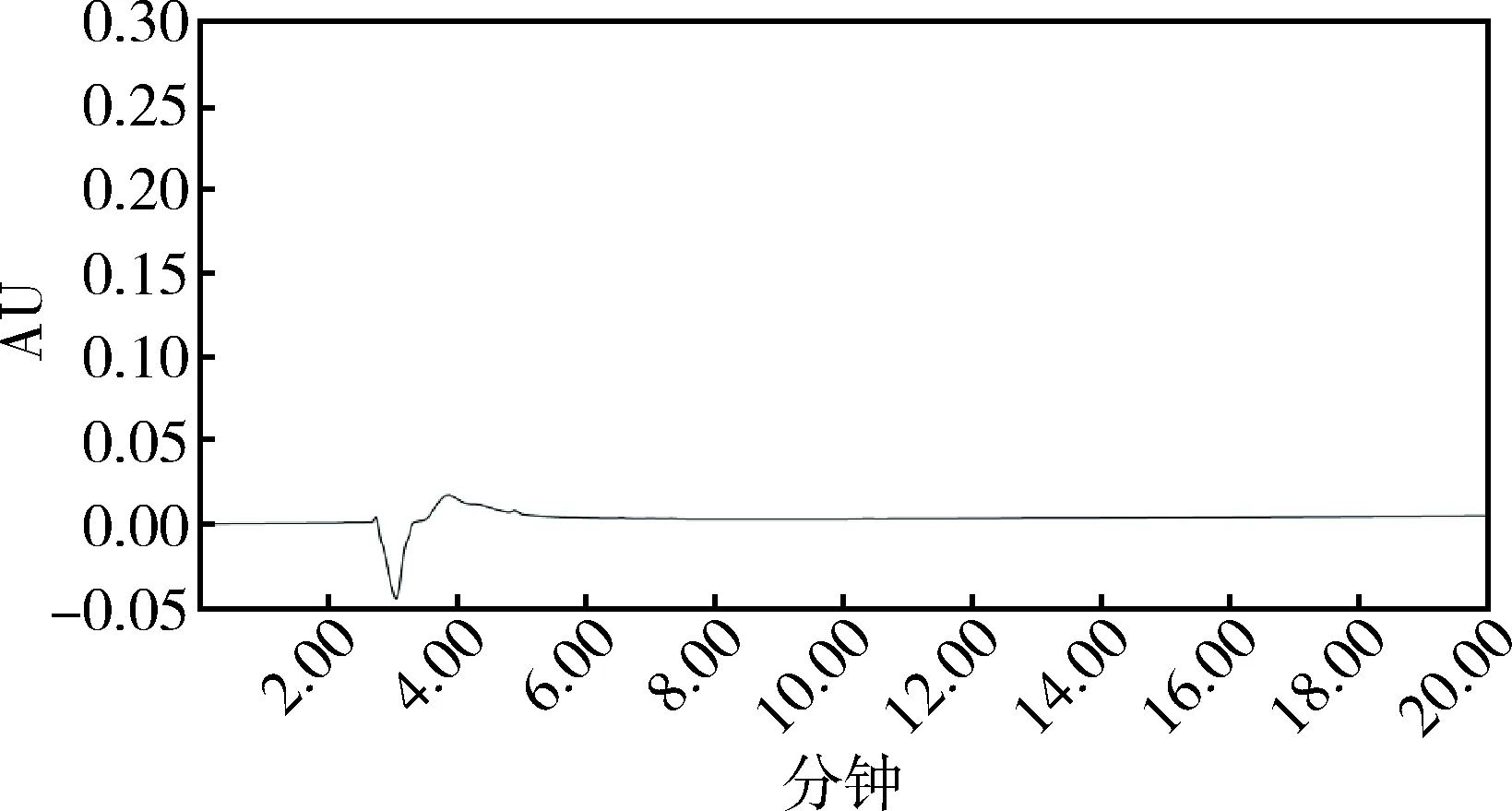
图3 溶剂空白液相色谱图Fig 3 Liquid chromatogram of solvent blank
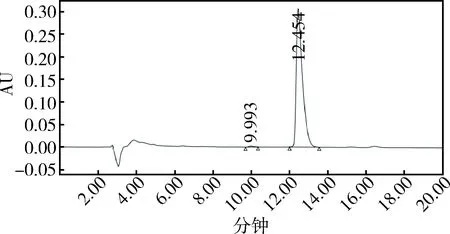
图4 泰拉霉素工作对照品液相色谱图Fig. 4 Liquid chromatogram of tulathromycin working reference substance
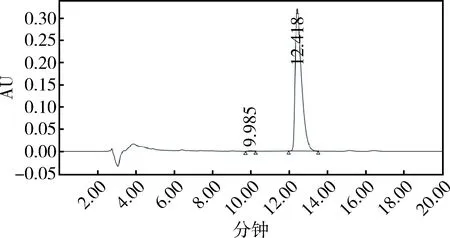
图5 本批泰拉霉素对照品液相色谱图Fig 5 Liquid chromatogram of this batch of tulathromycin reference substance
2.6 水分 按照《中国兽药典》2020年版一部附录0832费休氏法,取待标品3.0 g,精密称定,置于水分测定仪中,测定水分含量,结果为0.19%。
2.7 炽灼残渣 按照《中国兽药典》2020年版一部附录0841炽灼残渣检查法,精密称取本品1.0 g,置坩埚中,于750 ℃下炽灼至恒重,计算遗留残渣量,结果为0.09%。
2.8 残留溶剂 采用气相色谱法检测待标品合成工艺中使用的有机溶剂(庚烷、二氯甲烷、异辛烷)残留量。以 DB-624 毛细管柱(30 m×0.32 mm,1.8 μm) 为分离柱,以氮气为载气,柱温采用程序升温,起始温度40 ℃,维持5 min,再以20 ℃/min的速率升温至90 ℃,立刻以30 ℃/min的速率升温至225 ℃,维持2 min。顶空进样,平衡温度105 ℃,顶空平衡时间60 min,供试品溶液的质量浓度为30 mg/mL。采用外标法以峰面积计算。样品残留溶剂中仅检出异辛烷,残留量0.01%(图6~图8)。
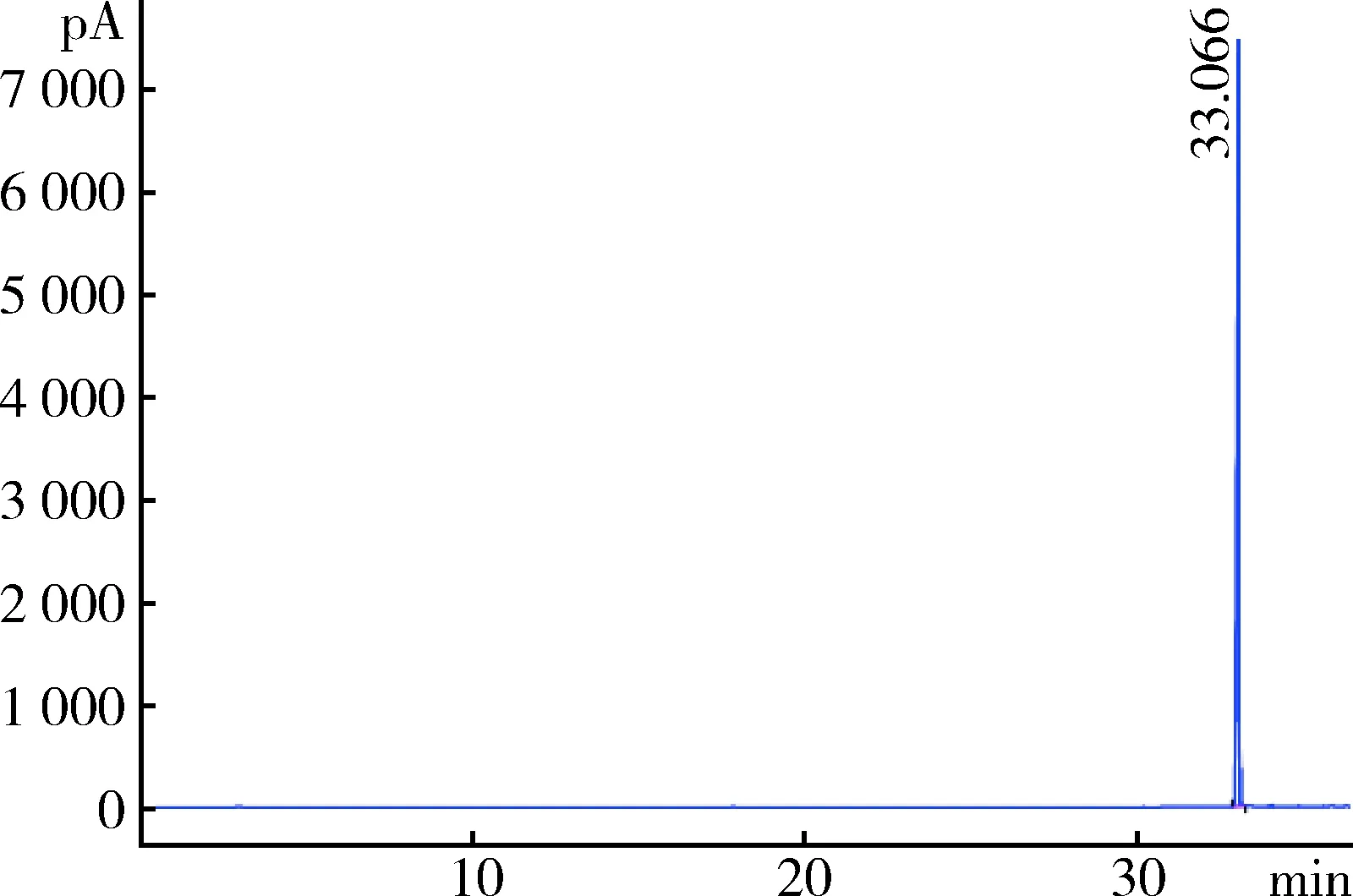
图6 溶剂空白气相色谱图Fig 6 Gas chromatogram of solvent blank
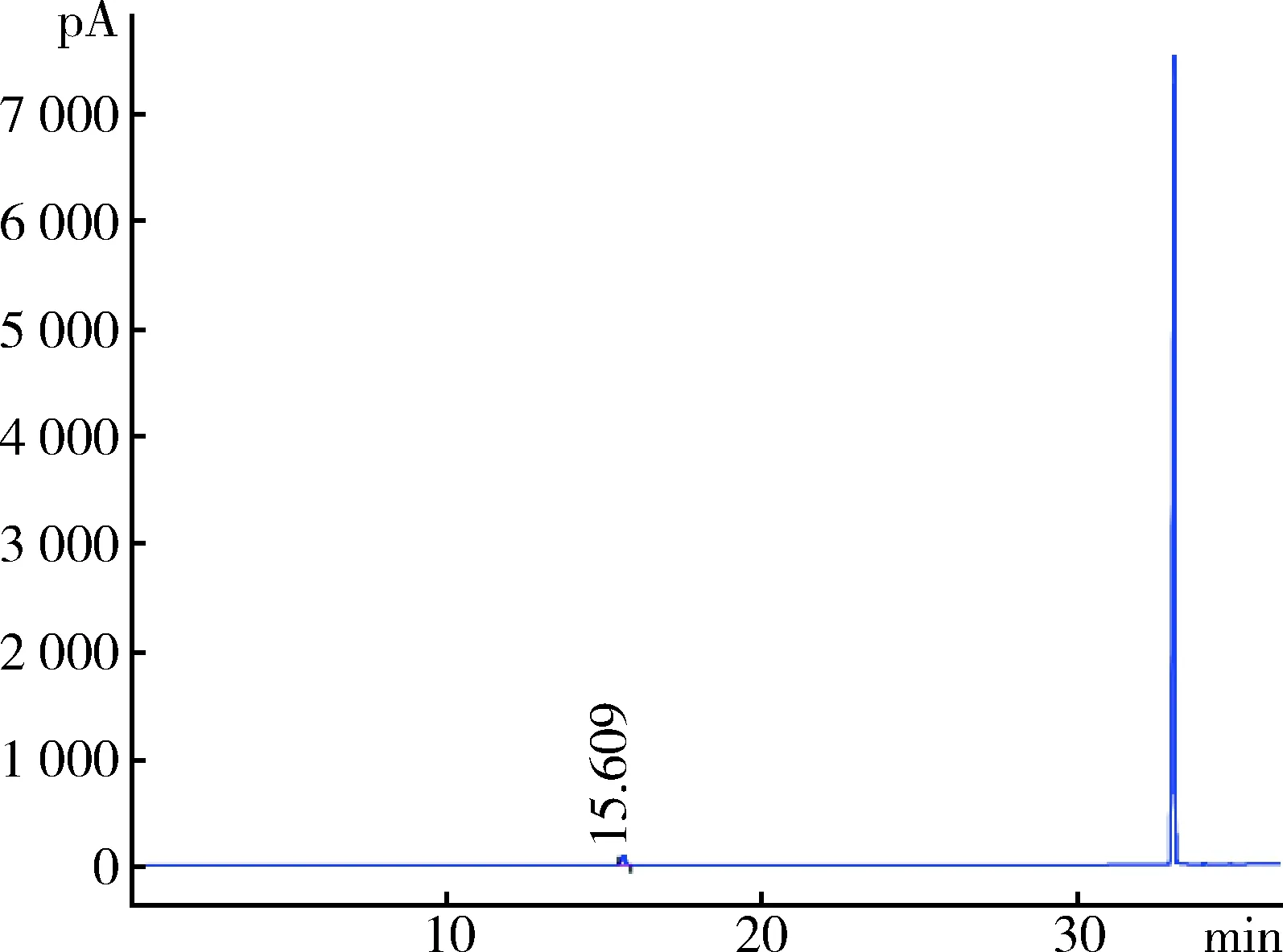
图7 异辛烷气相色谱图Fig. 7 Gas chromatogram of isooctane
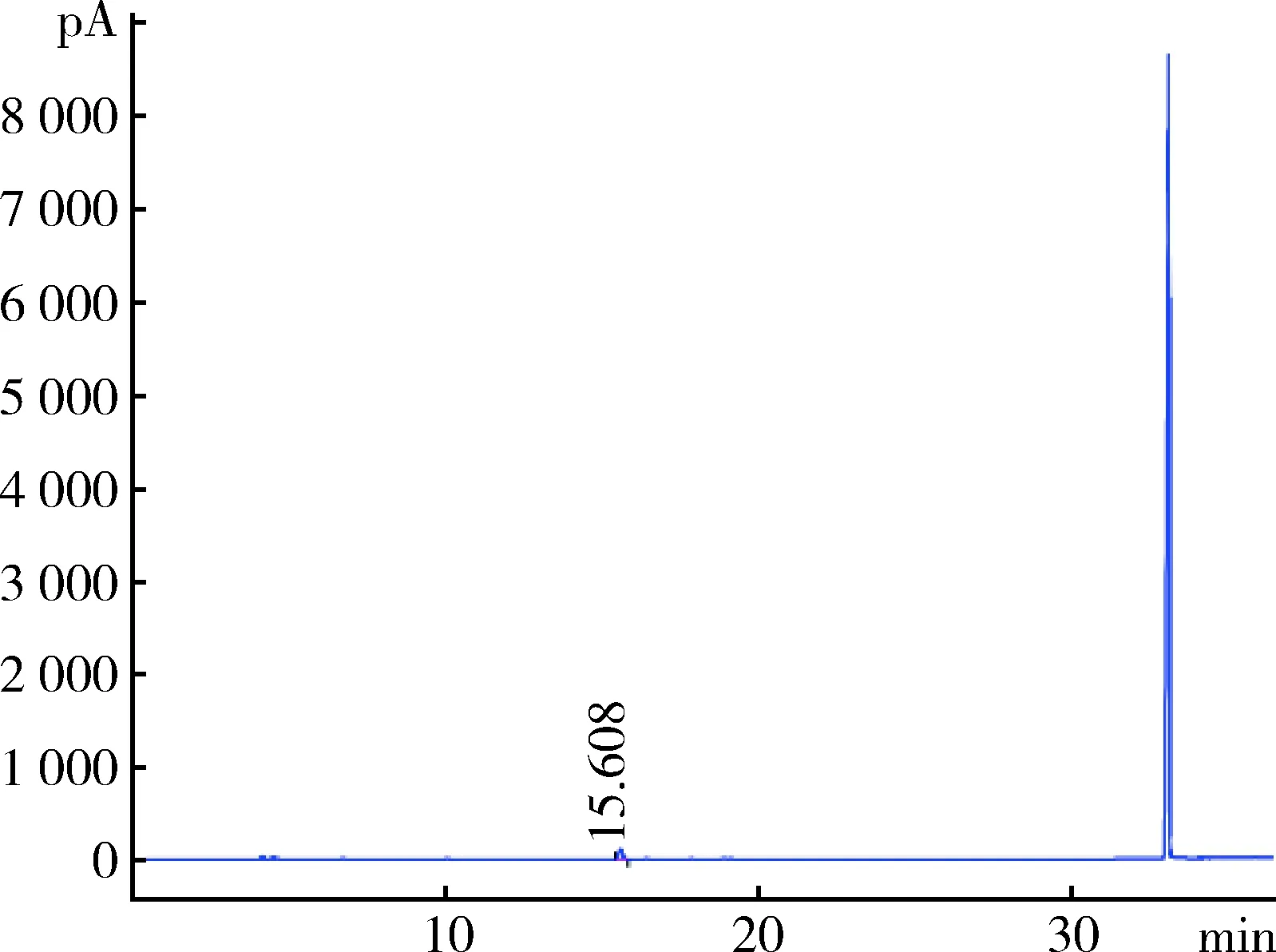
图8 本批泰拉霉素对照品气相色谱图Fig 8 Gas chromatogram of this batch of tulathromycin reference substance
2.9 均匀性评估 随机抽取待标品10支,每支取样2次进行测定,采用高效液相色谱法,按照2.4.1项下色谱条件,取本品20 mg,精密称定,制成质量浓度为2 mg/mL的溶液。以单位质量峰面积为结果,采用单因素方差分析法对测定结果进行均匀性评估。样品间自由度为9,样品内自由度为10,在约定自由度水平α=0.05的显著水平下,计算临界值F0.05(9,10),计算结果与查表得到的F临界值3.02比较,若计算值小于3.02,则表明在α=0.05的显著水平下,样品是均匀的。计算得样品均匀性单因素方差分析结果统计量F为2.60,小于3.02,表明研制的本批对照品均匀性良好,符合国家标准物质研制的要求。
2.10 含量测定
2.10.1 质量平衡法 根据质量平衡法的计算方法,采用以下公式计算泰拉霉素的含量:(1-有关物质)×(1-水分-残留溶剂-炽灼残渣)×100%。根据质量平衡法计算公式,计算得泰拉霉素含量为98.3%。
2.10.2 差示扫描量热法 采用差示扫描量热法对质量平衡法赋值结果进行验证。以不同升温速率,在175~210 ℃温度范围内测定待标品中泰拉霉素的含量,结果见表3,不同升温速率对测定结果影响不大。DSC法升温速率一般低于1 ℃/min时,体系接近平衡态,但有时为了节省时间和避免分解,可以用更快的升温速率,较快的升温速率有利于将分解效应与熔融效应分离。考虑到1 ℃/min升温速率图谱基线不平衡,因此选取了2 ℃/min和5 ℃/min的升温速率进行多次测定,泰拉霉素含量为98.5%,结果见表4,图谱见图9。
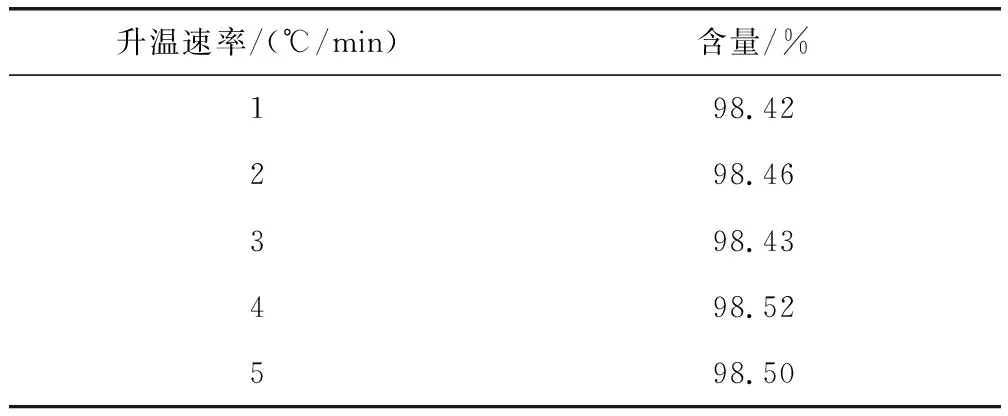
表3 不同升温速率样品含量Tab 3 Sample content at different heating rates
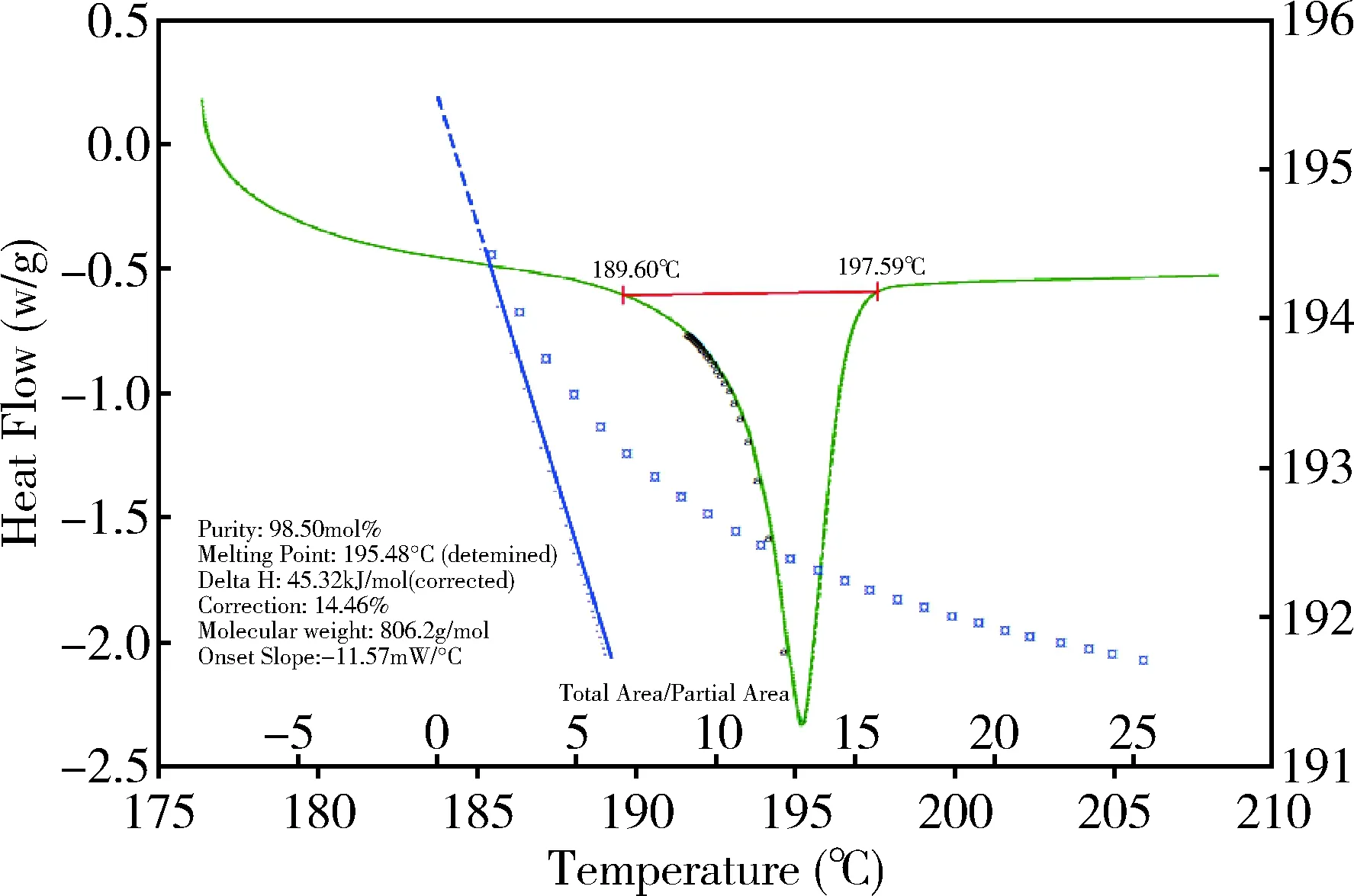
图9 本批泰拉霉素对照品差示扫描量热法图谱Fig 9 DSC atlas of this batch of tulathromycin reference substance
化学标准物质的定值目前较为普遍的方法是质量平衡法,其能够直接溯源到国际单位制中的质量单位,是国际上标准物质定值推荐的常用方法[4-5]。该方法赋值结果准确,但受影响因素较多,往往需要采用其他方法对质量平衡法的赋值结果进行验证[6]。差示扫描量热(DSC)法是研究应用最广泛的热分析技术之一,具备快速采集、操作简便等特点,越来越广泛地应用于标准物质的定值中[7-8]。本研究针对泰拉霉素样品的特点,在标定国家兽药标准物质的过程中,采用质量平衡法、差示扫描量热法分别对泰拉霉素进行定值与验证,确保定值结果的准确性。
本研究研制了泰拉霉素国家对照品,采用质量平衡法与差示扫描量热法两种不同原理的定值方法测定泰拉霉素含量,结果分别为98.3%和98.5%,两种方法标定结果基本一致,相互验证,可以保证定值的准确性。由于质量平衡法是世界卫生组织推荐的药品标准物质定值方法,能够更准确地反映本品的真实含量,因此,以质量平衡法的结果进行赋值,可作为国家对照品用于泰拉霉素及其制剂的含量测定。
猜你喜欢 定值霉素速率 圆锥曲线的一类定值应用中学生数理化(高中版.高二数学)(2022年1期)2022-04-26“大处着眼、小处着手”解决圆锥曲线中的定值问题新世纪智能(教师)(2021年2期)2021-11-05阿奇霉素辅助治疗呼吸道感染的临床效果医学前沿(2021年18期)2021-04-14桑叶中1-脱氧野尻霉素的抗病毒作用研究进展四川蚕业(2020年4期)2020-02-1010kV线路保护定值修改后存在安全隐患电子制作(2018年10期)2018-08-0410kV线路保护定值修改后存在安全隐患电子制作(2018年12期)2018-08-01莲心超微粉碎提高有效成分的溶出速率食品工业科技(2014年23期)2014-03-11服阿奇霉素两个“不必”恋爱婚姻家庭·养生版(2013年6期)2013-05-14核糖霉素祝您健康(1986年4期)1986-12-30